Развитие половых желез в эмбриогенезе обусловлено набором половых хромосом. Кариотин 46 ХХ определяет развитие яичников, а 46 ХY – яичек. Гонады, как мужские, так и женские, развиваются из 3 различных компонентов целомического эпителия, мезенхимы и примордиальных герминальных клеток.
Первичный зародыш гонад бипотенциален и состоит из 2 частей – кортикальной и медуллярной. При наличии двух функционально нормальных Х-хромосом кортикальная часть индифферентной гонады развивается в яичник. Гены, расположенные в перицентромерной области Y-хромосомы, определяют развитие медуллярной части в яичко.
Длительное время считалось, что гены, определяющие развитие бипотенциальной гонады в яичко, идентичны генам, которые кодируются как H-Y-антиген, являющийся клеточно-поверхностным белком, способным оказывать непосредственное действие на дифференцировку первичной гонады в яичко.
Однако тщательный анализ больных с различными нарушениями половой дифференцировки показали, что H-Y антиген не идентичен Y гену, контролирующему дифференцировку яичка. W.K. Silvers и соавт. (1982) четко установили, что H-Y антиген локализуется на длинном плече Y-хромосомы, достаточно далеко от гена, определяющего развитие пола плода. Детальное изучение карты хромосом у лиц с набором 46 ХХ-половых хромосом при наличии яичек и мужского фенотипа показало, что у них имеются определенные последовательности Y-хромосомы на Х-хромосоме. На основании этого было высказано предположение, что на Y-хромосоме имеется определенная последовательность, названная фактором, определяющим развитие яичка, которая локализовалась у этих больных на псевдоаутосомальной области. Ген, ответственный за развитие яичка, был идентифицирован D.C. Page и соавт. (1987) и клонированный ими участок хромосомы был назван ZFY. Указанная последовательность (ген ZFY) выявлялась у 46 ХХ фенотипичных мужчин, но отсутствовала у 46 XY фенотипичных женщин. Эти исследования позволили считать, что ZFY является небольшой частью Y-хромосомы, сочетающейся с дифференцировкой пола. Однако ZFY у некоторых больных определялся на аутосомах, а M.S. Palmer и соавт. (1990) описали 4 мужчин с 46 ХХ набором половых хромосом, у которых наследуемый участок Y хромосомы не включал ZFY, показывая, что ZFY не является фактором, ответственным за развитие яичка. Почти одновременно A.H. Sinclair и соавт. (1990) опубликовали уточняющие данные о локализации гена в области pY53.3, ответственного за пол организма, назвав его SRY (область Y-хромосомы, ответственная за определение пола). Этот ген, по их мнению, является истинным геном-кандидатом фактора или гормона, определяющего развитие яичка. Он экспрессируется только в яичках и отсутствует в легких и почках взрослого мужчины, как и в яичниках женщины. Область ДНК, в которой локализуется SRY, ответственна также за кодирование двух ключевых ферментов, участвующих в дифференцировке первичной гонады по мужскому типу: 1) ароматазы Р450,контролирующей конверсию тестостерона в эстрадиол и 2) фактора или гормона, ингибирующего развитие протоков Миллера, который вызывает обратное их развитие и способствует дифференцировке тестикул. Тем не менее SRY участвует в процессах половой дифференцировки в тесном взаимодействии с еще одним геном, названным K.McElreavey и соавт. (1993) геном Z, функция которого в норме заключается в угнетении специфических мужских генов. В случае нормального мужского генотипа 46XY ген SRY продуцирует белок, угнетающий ген Z, и специфические мужские гены активируются. В случае нормального женского генотипа 46ХХ, при котором отсутствует SRY, ген Z активируется и угнетает специфический мужской ген, что создает условия для развития по женскому типу. У 46ХХ мужчин также отсутствует ген SRY и это сопровождается активацией гена Z, соответственно угнетением специфического мужского гена, вызывая развитие по женскому типу. У мужчин с генотипом 46 ХХ и отсутствием SRY должна быть мутация Z гена, сопровождающаяся невозможностью экспресии Z гена, что и способствует при этом осуществлению дифференцировки по мужскому типу. Эта гипотеза также объясняет генез развития женского фенотипа при 46XY. У таких лиц имеется интактный ген SRY и, вероятно, мутация Z гена.
Дифференцировка наружных половых органов по мужскому типу происходит под влиянием тестостерона, который секретируется клетками Лейдига эмбриона. В клетках-мишенях (урогенитальный синус) должно быть достаточное количество рецепторов к тестостерону, наличием которых и объясняется чувствительность тканей к этому гормону. Гены, контролирующие синтез рецепторов к андрогенам, локализуются на Х хромосоме. C. Sultan и соавт. (1993) установили, что наличие у больных резистентности к андрогенам различной степени выраженности связано с мутациями гена рецептора к андрогенам. Рецепторы к андрогенам, как и другие рецепторы к стероидным и тироидным гормонам, состоят из гормонсвязывающего домена, ДНК-связывающего домена и N-концевого домена. Большинство мутаций при андроген-резистентных состояниях выявлены в гормонсвязывающем домене.
Следует указать, что в клетках – мишенях (урогенитальный синус и наружные гениталии) дифференцировку урогенитального синуса в наружные гениталии по мужскому типу опосредует не сам тестостерон, а его производное 5a-дигидротестостерон, который обладает большей биологической активностью. В цитозоле клеток-мишеней содержится фермент 5a-редуктаза (ген 5a-редуктазы расположен на 2-й хромосоме), которая переводит тестостерон в дигидротестостерон. Последний связывается высокоаффинным рецептором цитоплазмы и гормонорецепторный комплекс перемещается в ядро, взаимодействует с местами связывания на хроматине генома, что активизирует определенные гены и стимулирует синтез белков. Цитозольный рецептор, связывающий андрогены, регулируется геном, как указано выше, расположенным на Х-хромосоме.
Наряду с тестостероном важное значение в дифференцировке половых признаков отводится фактору, угнетающему развитие парамезонефрического протока (проток Мюллера), который секретируется клетками Сертоли эмбриона и под влиянием которого происходит инволюция протоков Мюллера, т.е. ингибируется их дифференцировка в матку и маточные трубы. Примордиальные герминальные клетки являются предшественниками сперматогоний в яичке и овоцитов в яичнике.
Дифференцировка бипотенциальной гонады в яичко начинается с процесса миграции примордиальных герминальных клеток на 7-й неделе (43-50-й день эмбрионального развития, когда длина плода составляет всего 13-20 мм) развития. Происходит трансформация интерстициальных поддерживающих клеток в клетки Сертоли, которые затем агрегируют (начинают соединяться друг с другом) и образуют семевыносящие канальцы. Для дифференцировки первичной гонады в яичко необходима также и нормальная функция клеток Сертоли, секретирующих, как указано, антимюллеров гормон, под влиянием которого у эмбриона мужского пола ингибируется развитие протоков Мюллера и они подвергаются обратному развитию. Ген, ответственный за синтез антимюллерова гормона, локализуется на 19-й хромосоме.
Клетки Лейдига дифференцируются из мезенхимы уже на 9-й неделе внутриутробного развития и способны секретировать тестостерон, содержание которого увеличивается с пиком на 15-18-й неделе. Эти клетки имеют рецепторы, связывающие как ЛГ, так и хорионический гонадотропин, под влиянием которого осуществляется биосинтез тестостерона. Секреция тестостерона в период эмбрионального развития имеет прямую корреляцию с уровнем хорионического гонадотропина. Лишь позже гипофиз плода начинает секретировать ЛГ, обеспечивая вместе с хорионическим гонадотропином нормальную секрецию тестостерона, дифференцировку урогенитального синуса, рост и развитие наружных мужских половых органов.
Таким образом, для нормального мужского фенотипа необходима интактная Y хромосома с локализацией на ней генов SRY и Z, нормальная функция Х хромосомы с наличием на ней гена, ответственного за рецепторы к андрогенам. Для последующей дифференцировки организма по мужскому типу необходимы также не только секреция тестостерона клетками Лейдига и секреция клетками Сертоли фактора, угнетающего развитие протока Мюллера, но и наличие в клетках-мишенях 5a-редуктазы, цитозольных рецепторов к андрогенам в протоках Вольфа, урогенитальном синусе и наружных гениталиях, мембранных рецепторов, связывающих фактор, угнетающий развитие протока Мюллера, и, естественно, наличие интактного андрогенрегулируемого гена транскрипции белков. Дефект в любом звене этого механизма приведет к нарушению половой дифференцировки и развитию организма по женскому типу.
При отсутствии Y-хромосомы и наличии кариотипа 46 ХХ примордиальные герминальные клетки развиваются в яичник. Это происходит на 17-20-й неделе эмбрионального развития, когда примордиальные герминальные клетки образуют овоциты, окруженные слоем гранулезных клеток (аналог клеток Сертоли в яичке). Количество их достигает максимума (6,2-6,7 млн.) на 5-м месяце эмбрионального развития, а затем начинает снижаться и к периоду рождения количество герминальных клеток составляет около 2 млн. К 7-летнему возрасту количество овоцитов уменьшается до 300 тыс. При наличии только одной Х хромосомы (45Х0) овоциты яичника подвергаются дегенерации еще до рождения. Вторая Х хромосома необходима не для дифференцировки первичной гонады в яичник, а для поддержания массы яичника и его дальнейшего развития. Было показано, что на Х хромосоме имеются два локуса (один на коротком плече Х хромосомы – Хр 11.2-R11.4 и второй на длинном плече Х хромосомы – Xq 11/3 или Xq21, возможно также Xq25 или Xq26), ответственные за поддержание и развитие яичника. Протоки Мюллера образуют репродуктивные органы женщины: маточные трубы, матку и верхнюю 1/3 влагалища. Влагалище, вернее его 2/3, является производным урогенитального синуса. Наружные гениталии претерпевают незначительные изменения.
Мужские половые железы (яички) являются местом образования и секреции тестостерона и местом сперматогенеза, который осуществляется в извитых канальцах, выстланных клетками Сертоли, первичными половыми клетками – сперматогониями. Из сперматогоний через стадии образования сперматоцитов первого и второго порядка развиваются сперматозоиды. Клетки Сертоли, содержащие жировые и пигментные зернышки, являются питающими сперматозоиды клетками.
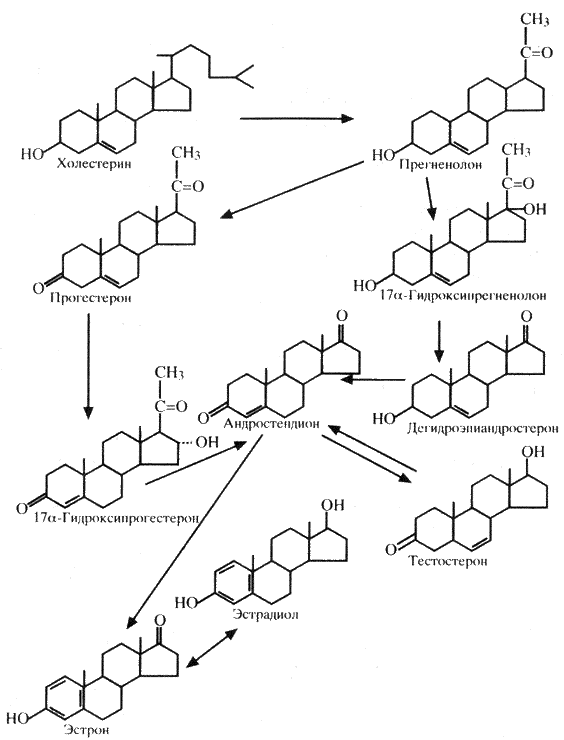
Секреция тестостерона осуществляется клетками Лейдига, которые расположены в промежуточной ткани яичка. Небольшое количество гормона секретируется корой надпочечника, а в женском организме – яичниками. Биосинтез тестостерона осуществляется следующим путем: ацетат ё холестерин ё прогненолон ё прогестерон ё 17a-гидроксипрогестерон ё андростендион ё тестостерон. Возможен и другой путь: из прегненолона через стадию 17a-гидроксипрегненолона (или минуя эту стадию) образование дегидроэпиандростерона ё андростендиона ё тестостерона. Аналогичные ферментативные реакции происходят в коре надпочечника и яичниках.
Синтезированный в яичках тестостерон поступает в кровь и лимфу. Поступивший в кровь тестостерон конвертируется (частично в крови, а большей частью – в периферических тканях) в дигидротестостерон, который обладает большей биологической активностью. Тестостерон является своего рода прогормоном для дигидротестостерона.
В крови тестостерон и дигидротестостерон связываются белками, главным образом глобулином. Глобулин, связывающий половые гормоны, образуется в печени и имеет молекулярную массу около 100 000 дальтон. При циррозе печени, гипертирозе и гипогонадизме у мужчин уровень глобулина, связывающего половые гормоны, в сыворотке крови повышен. Концентрация этого глобулина в крови является основным фактором, определяющим баланс между андрогенами и эстрогенами. Около 98% тестостерона в крови находится в связанном с глобулинами состоянии, а остальное его количество (около 2%) является свободным, способным связываться рецепторами тканей-мишеней и оказывать биологическое действие. Глобулин, связывающий половые гормоны, имеет большее сродство к тестостерону, чем к эстрогенам.
В препубертатном периоде концентрация глобулина, связывающего половые гормоны, одинакова у мальчиков и девочек; в период полового созревания у лиц мужского пола наблюдается более значительное снижение его уровня, а у женщин концентрация этого глобулина в крови в 2 раза выше по сравнению с его уровнем в сыворотке крови мужчин. Известно, что концентрация тестостерона в крови у мужчин в 20 раз выше по сравнению с его уровнем у женщин, однако уровень свободного тестостерона у мужчин выше в 40 раз. У мужчин скорость образования тестостерона составляет 6-7 мг в сутки, концентрация в крови 8,5-27 нмоль/л, у женщин – около 1 мг в сутки и уровень в крови 0,6-1,9 нмоль/л. Разрушение тестостерона под влиянием 17b-дегидрогеназы происходит в основном в печени, где его метаболиты связываются с глюкуроновой и серной кислотами и эксретируются с мочой в виде 17-кетостероидов, которые представлены андростероном, эпиандростероном, этиохоланолоном и дегидроандростероном.
Функция яичек находится под влиянием гонадотропных гормонов передней доли гипофиза. Фоллитропин (ФСГ) стимулирует сперматогенный эпителей, а лютропин (ЛГ, гормон, стимулирующий интерстициальные клетки) – секрецию тестостерона. Уровень тестостерона в сыворотке крови мальчиков увеличивается в период полового созревания, а после 50 лет имеет тенденцию к снижению, что сопровождается повышением ФСГ и ЛГ в сыворотке крови. Уровень тестостерона в сыворотке крови, как и глюкокортикоидов, изменяется на протяжении суток. Наибольшее повышение отмечается в 7-9 ч утра, самый низкий уровень – в 24 и 3 ч утра.
Тестостерон и другие андрогены, ответственные за формирование вторичных мужских половых признаков (оволосение на лице, в подмышечных впадинах, рост гениталий и т.д.), обеспечивают либидо и потенцию, обладают анаболической активностью, стимулируют рост скелета и всех тканей организма, что проявляется увеличением массы тела и объема мышц, ускоряют созревание скелета.
В яичках секретируется около 1/3 эстрогенов сыворотки крови. Остальная часть их образуется в печени вследствие конверсии тестостерона. Мужчины в возрасте 20-40 лет экскретируют с мочой в сутки 3,7 мкг эстрона, 0,8 мкг эстрадиола и 3,4 мкг эстриола.
Женские половые железы – яичники – являются местом образования и секреции женских половых гормонов (эстрогены и прогестерон), ответственных за развитие вторичных половых признаков, рост и созревание женских гениталий, стимулируют рост и созревание скелета, способствуют отложению подкожной жировой клетчатки, характерной для женского организма, контролируют менструальный цикл.
Наряду с образованием эстрогенов и прогестерона яичники секретируют незначительное количество андрогенов.
Эстрогены. Секретируются клетками внутренней оболочки (theca interna) везикулярного яичникового фолликула (граафова пузырька) и зернистой оболочкой (ctratum granulosum). Биосинтез стероидов в яичнике представлен на схеме 36.

Эстрон и эстрадиол являются гормонами, которые образуются в яичнике. Биологически наиболее активен эстрадиол, 95% которого образуется в фолликуле, и уровень его в крови является показателем созревания фолликула. Эстриол – метаболит эстрадиола и эстрона, обладающий наименьшей биологической активностью. Секретируемые в кровь эстрогены конъюгируются глобулином, связывающим половые гормоны, и в меньшей степени альбуминами крови. Выше указывалось, что этот глобулин имеет повышенное сродство к андрогенам. Уровень глобулина, связывающего половые гормоны, в сыворотке крови женщин почти в 2 раза выше по сравнению с его концентрацией в крови мужчин. Эстрогены и их метаболиты конъюгируются в печени с глюкуроновой и серной кислотами и экскретируются с желчью и мочой.
Влияние эстрогенов на гипоталамо-гипофизарную систему обеспечивает цикличность выделения гонадотропинов.
Эстрогены угнетают секрецию ФСГ и ЛГ, а также снижают ответ передней доли гипофиза на действие гонадолиберина.
Кроме влияния на половые органы и гипоталамус, эстрогены обладают анаболическим свойством, усиливают обмен костной ткани и ускоряют созревание костей скелета, с чем связано прекращение роста при наступлении полового созревания. В больших дозах эстрогены способствуют задержке натрия и воды в организме вплоть до развития отеков. Влияют также на обмен липидов, снижая уровень холестерина в крови. Длительное применение эстрогенов способствует тромбообразованию в венах, а также увеличивает частоту рака эндометрия. Эстрогены не являются канцерогенами, но, инициируя процессы пролиферации эндометрия, вероятно, создают условия для действия неизвестных пока канцерогенов и злокачественного перерождения тканей.
Прогестерон. Секретируется желтым телом, а также корой надпочечников и яичками, где используется как предшественник для биосинтеза кортикостероидов и андрогенов. В сыворотке крови прогестерон связывается транскортином, который, как известно, связывает глюкокортикоиды. По данным некоторых исследований, способность прогестерона связываться транскортином даже выше, чем кортикостероидов. Следует отметить, что синтетические кортикостероиды, такие, как дексаметазон, вообще не связываются транскортином. В печени прогестерон связывается глюкуроновой кислотой, конъюгаты экскретируются с мочой.
Прогестерон, являясь анатагонистом эстрогенов, ограничивает их пролиферативный эффект в эндометрии, миометрии и эпителии влагалища, вызывая стимуляцию секреции железами эндометрия секрета, содержащего гликоген, уменьшая строму подслизистого слоя, т.е. вызывает характерные изменения эндометрия, необходимые для имплантации оплодотворенной яйцеклетки. Прогестерон снижает тонус мышц матки, вызывает их расслабление, оказывает пирогенное влияние. Увеличение его содержания в крови совпадает с повышением базальной температуры тела, которая является индикатором овуляции. Кроме того, прогестерон вызывает пролиферацию и развитие молочных желез и в период беременности способствует угнетению процесса овуляции. Обладает небольшим катаболическим эффектом, при длительном применении способстует появлению акне, олигоменореи, задерживает натрий, хлориды и воду в организме.
В последние годы показано, что яичники являются местом секреции полипептидного гормона релаксина, который принимает важное участие в период родов, вызывая релаксацию связок таза и расслабление шейки матки, а также увеличивает синтез гликогена и задержку воды в миометрии, уменьшая при этом его сократительную способность. Он секретируется клетками гранулезы желтого тела. В период обычного менструального цикла секреция его повышается сразу после пика высвобождения ЛГ и остается определяемым в период менструации. В течение беременности циркулирующий уровень релаксина выше в конце I триместра по сравнению со II и III триместром.
Помимо релаксина, в яичнике секретируются ингибин и активин, которые участвуют в регуляции секреции ФСГ и модулируют секрецию стероидных гормонов клетками яичника.
Андрогены. У женщин секретируются клетками стромы яичников, главным образом в виде андростендиона, причем в надпочечниках его образуется в 3 раза больше, чем в яичниках. Андростендион в периферических тканях конвертируется в тестостерон. В яичниках образуется в незначительных количествах также тестостерон, дигидротестостерон, дегидроэпиандростерон. Приблизительно около 1/4 тестостерона, который секретируется в организме женщины, образуется в яичниках. Остальное его количество секретируется надпочечниками или образуется в тканях на периферии путем конверсии из андростендиона. В этой связи потеря вторичного оволосения у женщин является индикатором надпочечниковой, а не яичниковой недостаточности. Повышение секреции андрогенов яичниками наблюдается при таких патологических состояниях, как синдром поликистозных яичников и арренобластома.
Биологическое действие стероидов, в том числе половых, в тканях-мишенях связано с наличием в них специфических рецепторов. Стероиды путем диффузии проходят мембрану клетки и в цитозоле комплексируются со специфическими рецепторами. Цитоплазматические рецепторы присутствуют не во всех, а только в клетках тканей, чувствительных к данному виду гормона. Рецепторно-стероидный комплекс, образование которого зависит от нескольких факторов, включая температуру, перемещается в ядро, где на хроматине имеются специальные участки, связывающие эти комплексы. Последнее взаимодействие ведет к синтезу большого количества специфических РНК и соответствующих белков, росту и развитию соответствущих органов и тканей (молочные железы, матка и др.).
Количество молекул рецепторов для различных стероидных гормонов колеблется от 5000 до 20 000 на клетку. Рецепторы к эстрогенам связывают многие естественные и синтетические эстрогенные стероиды с одинаковой аффинностью. Считается, что рецепторы к эстрогенам и прогестерону представляют собой две субъединицы, каждая из которых связывает молекулу гормона. Каждая из таких субъединиц А и В взаимодействует с хроматином и обеспечивает дальнейшую активацию специфических генов и РНК-полимераз.
Биологическое действие гормона связано не только с количественными колебаниями его в сыворотке крови, но и с состоянием рецепторного звена, причем количество рецепторов подвержено значительным колебаниям. Экспериментальные исследования показали, что у новорожденных крыс ткани-мишени содержат незначительное количество рецепторов к эстрогенам. На 10-й день жизни количество рецепторов возрастает, и после этого срока введение экзогенных эстрогенов вызывает их увеличение. Эстрогены стимулируют образование рецепторов не только к эстрогенам, но и к прогестерону. Количество рецепторов не только зависит от уровня циркулирующего в крови гормона, но и находится под генетическим контролем. Так, полное отсутствие рецепторов к андрогенам наблюдается при синдроме тестикулярной феминизации.
При некоторых состояниях, проявляющихся резистентностью к андрогенам, имеется нормальное комплексирование андрогенов с цитозольным рецептором, но связывание гормонорецепторного комплекса на хроматине ядра нарушено. Действие различных антигормонов связано со способностью этих веществ взаимодействовать со специфическим рецептором. Так, синтетические антиэстрогены (нафоксидин и тамоксифен) связываются с цитоплазматическим рецептором, и такой рецепторно-гормональный комплекс, транслоцируясь в ядро, связывается с хроматином на более продолжительное время (дни и недели), чем при комплексировании с эстрадиолом.
Гормональная регуляция менструального цикла. Секреция эстрогенов и прогестерона находится под контролем гонадотропных гормонов. Уже на самых ранних стадиях развития фолликула зависит от стимулирующего влияния ФСГ. Гонадотропины стимулируют созревание, разрыв фолликула и его трансформацию в желтое тело. Образование эстрогенов стимулируется преимущественно ФСГ, однако при этом необходим определенный фон секреции ЛГ, без чего ФСГ малоактивен. Функция желтого тела находится преимущественно под влиянием ЛГ. Гипоталамический контроль секреции гонадотропных гормонов был рассмотрен в главе I. Секреция гонадотропных гормонов находится под контролем не только ЦНС и гипоталамуса. Половые гормоны посредством положительной или отрицательной обратной связи также принимают важное участие в регуляции секреции гонадотропинов.
Существуют 3 типа секреции гонадотропинов: тонический, циклический и эпизодический, или пульсирующий. Тоническая, или базальная, секреция гонадотропинов регулируется посредством отрицательной обратной связи, а циклическая – механизмом положительной обратной связи с участием эстрогенов. Пульсирующая секреция обусловлена активностью гипоталамуса и высвобождением гонадолиберина. Развитие фолликула в первой половине цикла осуществляется благодаря тонической секреции ФСГ и ЛГ. Повышение секреции эстрадиола приводит к торможению образования ФСГ. Развитие фолликула зависит от количества рецепторов к ФСГ в клетках гранулезной зоны, причем синтез этих рецепторов в свою очередь стимулируется эстрогенами.
Таким образом, ФСГ приводит к синтезу в определенном фолликуле эстрогенов, которые, увеличивая количество рецепторов к ФСГ, способствуют накоплению ФСГ (путем связывания его рецепторами), дальнейшему созреванию фолликула и увеличению секреции эстрадиола. Другие фолликулы в это время подвергаются атрезии. Концентрация эстрадиола в крови достигает масимума в предовуляторный период, что приводит к высвобождению большого количества гонадолиберина и последующего пика высвобождения ЛГ и ФСГ. Предовуляторное повышение ЛГ и ФСГ стимулирует разрыв граафова пузырька и овуляцию.
Оставшаяся гранулезоклеточная ткань гипертрофируется и гиперплазируется, превращаясь в желтое тело, которое начинает секретировать прогестерон. Эта фаза, продолжительность которой составляет 13±1 день, носит название лютеиновой. Уровень прогестерона увелчивается в 10-20 раз по сравнению с фолликулярной фазой и достигает максимума на 20-25-й день цикла. Если не произошло оплодотворения яйцеклетки, секреция прогестерона резко уменьшается за 1-2 дня до начала менструации. Во время менструации наблюдается дальнейшее снижение уровня прогестерона и эстрадиола в крови, что приводит к стимуляции секреции ФСГ и ЛГ и началу нового цикла.
Повышение уровня ФСГ стимулирует развитие сразу нескольких первичных фолликулов (10-15), но посредством внутрияичникового саморегулирующегося механизма наступает созревание лишь одного и одновременная атрезия других фолликулов. В том случае, если предовуляторное повышение эстрадиола не приводит к высвобождению гонадолиберина и последующей секреции ЛГ и ФСГ, происходит так называемый ановуляторный цикл. Следует отметить, что одновременно с секрецией эстрадиола увеличивается образование 17a-гидроксипрогестерона клетками внутреннего слоя граафова пузырька, который вместе с эстрадиолом способствует циклической секреции гонадотропинов.
Под влиянием эстрогенов в фолликулярной фазе цикла в эндометрии происходят пролиферативные процессы (фаза пролиферации) – разрастание желез, стромы и сосудов, которые постепенно восполняют отторгнувшийся функциональный слой эндометрия. Во второй (лютеиновой) фазе цикла под влиянием прогестерона в эндометрии развиваются секреторные процессы (фаза секреции), которые характеризуются тем, что железы эндометрия начинают вырабатывать секрет, содержащий мукоид, глюкоген, необходимый для имплантации оплодотворенного яйца. В этот период под влиянием высокого уровня прогестерона повышается базальная температура тела. В случае отсутствия оплодотворенной яйцеклетки наступает менструация, которая продолжается 3-7 дней.
Необходимо отметить, что созревание фолликула и его трансформация в желтое тело осуществляются не только под влиянием ФСГ и ЛГ. Нормальная реакция яичников на ФСГ и ЛГ происходит при наличии определенной секреции катехоламинов и образования простагландинов F и E.
Яичники, таким образом, секретируют 3 класса стероидов: эстрогены, андрогены и прогестины. Фолликул яичника является местом образования гормонов и андрогены продуцируются клетками theca interna, которые экспрессируют 17a-гидроксилазу цитохрома Р450. Этот фермент необходим для конверсии прегненолона в 17a-гидроксипрегненолон и дегидроэпиандростерон и для конверсии прогестерона в 17a-гидроксипрогестерон. В клетках зернистой оболочки (клетки гранулезного слоя) экспрессируется фермент – ароматаза цитохрома Р450, необходимая для конверсии образующихся андрогенов в эстрогены. В клетках внутренней и зернистой оболочки экспрессируется два фермента: 1) фермент 20,22 десмолаза, участвующий в отщеплении боковой цепи в молекуле холестерина и конверсии ее в прегненолон и 2) 3b-гидроксистероидная дегидрогеназа, необходимая для конверсии прегненолона в прогестерон и дегидроэпиандростерона в андростендион. Гонадотропины (ФСГ и ЛГ) регулируют секрецию всех яичниковых стероидов в течение менструального цикла.
Как показано исследованиями последних лет, в реализации биологических эффектов гонадотропинов участвуют несколько факторов роста: ИФР-I (инсулиноподобный фактор роста -I), трансформирующий фактор роста-a и b, фактор роста фибробластов, эпидермальный фактор роста.
Кроме того, в последние годы установлено, что жидкость, находящаяся в полости созревающего фолликула, содержит несколько пептидных гормонов, участвующих в сложных процессах регуляции созревания яйцеклетки, овуляции и функциональной активности желтого тела. Одним из таких белковых гормонов является ингибин, угнетающий секрецию ФСГ. Ингибин состоит из двух почти гомологичных субъединиц (a- и b-субъединицы) и их различная комбинация представлена в ингибине А (a и bА) и ингибине В (a и bВ). Как показали D.M. Robertson и соавт. (1997), мол.м. ингибина А 33-36 кD, а ингибина В -50-66 кD.
Активины, как и ингибины, относятся к семейству трансформирующего фактора роста-b, они также были изолированы из фолликулярной жидкости и секретируются лютеальными и клетками зернистого слоя. Активины оказывают биологическое действие в различных тканях. В яичниках они снижают образование андрогенов, прогестерона и активность ароматазы.
Фоллистатин является гликопротеидом и также был изолирован из фолликулярной жидкости и подобно ингибину уменьшает высвобождение ФСГ в культуре гонадотропных клеток гипофиза. Кроме того, он имеет высокую аффинность к связыванию активина и менее выраженную к связыванию ингибина. Установлено, что фоллистатин и активин А являются компонентами аутокринно-паракринной системы фолликула и участвуют в регуляции различных функций клеток внутренней оболочки граафова пузырька.
Самая свежая информация коррекция вросшего ногтя на сайте.